
發布者:禹州華德|2022-07-08| 返回列表
隨著我國人口的增加以及人民生活水平的提高,對工農業的發展需求也逐漸增加,因此導致水資源量在供需方面不平衡,且由此造成的水環境污染也越來越嚴重,據相關學者研究,解決這種現象最根本的辦法就是開源節流,就是要求我們最大限度的做好廢水的回收利用,向人們灌輸節約用水的觀念。工業的發展必須要有充足的能源供應作為保障,據報道,礦產資源是我國能源供應的主力軍,從2010-2015年我國共產煤102.3億t,2016-2017年就產煤45.6億t,產煤量以每年8.3%的速率快速增長,近年來我國雖在不斷調整能源供應的結構,目前也是多能源供應,煤炭雖是一次性能源,但由于價格低廉且產量多,在未來很長一段時間之內其主力軍地位仍無其他能源可以替代。隨著煤礦的不斷開采,由此造成的環境污染問題也越發嚴重,煤礦廢水具有pH值不穩定、懸浮物濃度高、鹽度高、水質復雜等特點,煤礦廢水的來源主要有:礦區的生活廢水、煤礦礦井廢水、選煤廢水以及煤制氣廢水等,其中礦井廢水主要是采礦時會擾動地下水沉,因此必須做好礦井的排水工作;選煤廢水主要是日常工藝和管理過程中對煤泥水要求循環利用外排所產生的泥水,這類廢水一般懸浮物濃度較高,含有大量的溶解性固體和放射性元素等;煤制氣廢水主要來自工藝中煤氣出口的豎管和洗滌塔冷凝后的廢水,這類廢水具有懸浮物濃度高,有機物和無機物含量高等特點。
煤礦廢水主要有酸性廢水(pH<6.5)、中性廢水(ph介于6.5和8.5之間)以及堿性廢水(ph>8.5),但大部分的煤礦廢水還是呈中性,北方地區的煤礦主要為弱堿性或者中性廢水,南方地區的煤礦主要為弱酸性和中性廢水,我國煤礦的礦井廢水主要包括潔凈廢水、高懸浮物礦井廢水、高鹽度廢水、酸性礦井廢水、甚至有些含放射性物質的廢水(如鐳、鈾),含重金屬物質的礦井廢水(如鐵元素)等。煤礦廢水處理時應根據開采規模、排水水質要求以及廢水的水質特征等方面綜合考慮選用最適合和經濟的工藝,目前有關這方面的研究較多,應用最多的還是混凝、沉淀、過濾、消毒、反滲透、電析等方面,因煤礦廢水一般具有鹽度高等特點,而混凝工藝對于處理高鹽度廢水具有較大的優越性,近年來在這方面的研究興起較快,針對具體煤礦特征,混凝時要求添加適宜量的混凝劑和助凝劑,用量選取的合適與否關系到廢水硬度和廢水中硫酸的去除效果,本文擬選取山西朔州懷仁礦區廢水作為研究對象,采用自行設計的混凝工藝,研究混凝工藝處理該礦區廢水需添加的混凝劑和助凝劑量最佳用量,研究結果可為進一步了解混凝工藝的處理機理提供理論參考。
1、工藝流程以及試驗方法
工藝流程如圖1所示。
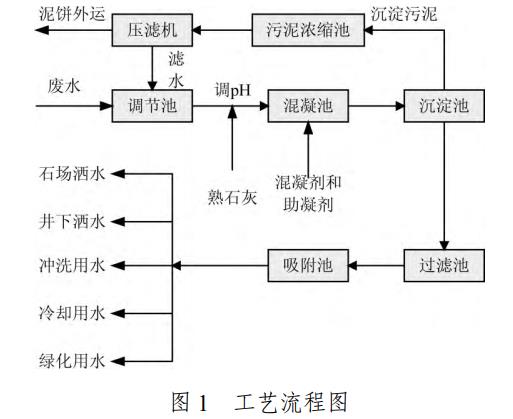
廢水依次流經調節池、混凝池和沉淀池,沉淀池后對于沉淀的污泥經過污泥濃縮池濃縮后的污泥用壓濾機壓縮,壓縮后的泥餅再外運,對于沉淀池中的水后續流經過濾池和吸附池后被循環利用,由于廢水中pH為酸性,廢水經調節池進入混凝池之前先加熟石灰調節pH至中性,在混凝池中添加混凝劑(PAC、PAF),本試驗中所需用到的試驗設備見表1。

廢水水質如表2所示,其中pH采用pH試紙測,溫度采用溫度計測量,懸浮物(SS)采用濾膜過濾后稱重,配置EDTA標準溶液,添加絡黑T固體為指示劑,根據酸堿滴定原理測定水的硬度和鈣元素(Ca)、鎂元素(Mg)含量,添加氯化鋇溶液根據沉淀滴定法測定水中硫酸根離子(SO42)含量,采用原子吸收分光光度法測定銅(Cu)元素含量,紫外分光光度法測定硝酸根(NO3-)含量,分子吸收光譜法測定鐵元素(Fe)含量,采用莫爾法測定水中氯元素含量,樣品檢測時嚴格按照《水和廢水監測分析方法》中相關步驟及操作規范進行。
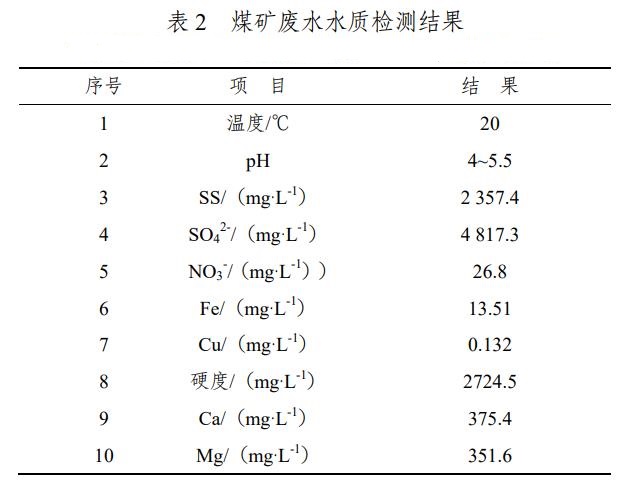
從表2可知:廢水呈酸性,故應加熟石灰(Ca(OH)2)調節pH至中性,SS濃度較高、硬度、Ca、Mg和SO42-含量較高,其他檢測的元素濃度值不是很高,又因Ca、Mg元素含量反映的就是硬度,故下文只對SO42-含量、SS和硬度進行分析,SS是在整個工藝過程中逐步去除,而SO42-含量和硬度主要在混凝過程中去除,故下文分析各池子內的SS濃度變化情況和混凝過程中添加的最適宜Ca(OH)2用量、混凝劑的用量。
2、結果與分析
2.1 混凝機理分析
混凝主要是在廢水中添加化學物質使水中的膠體粒子或者懸浮物聚集,主要包括兩個過程(凝聚和絮凝過程),其作用機理也是凝聚和絮凝機理,目前有關混凝機理方面的認識主要有:壓縮雙電層作用、卷掃作用和電中和作用。壓縮雙電層特有的結構,決定著膠體之間表面處的反離子濃度是所有位置中最大值,當顆粒之間較為分散時,顆粒之間的反離子濃度逐漸減小,直到和溶液濃度值相等,當水中添加混凝劑后,廢水中的擴散層減小,反離子濃度增加,離子電位也相應的降低,因為擴散層的厚度變小了,粒子之間的排斥作用也減少了,當顆粒之間相互凝結碰撞時,因顆粒之間距離減少了,分子之間的引力也會增加,引力大于排斥力,隨后顆粒之間得以聚集而沉淀;當膠體表面吸附了相關的異處離子、膠體顆粒或分子時,這些粒子可以中和自身所帶的電荷,也減少了粒子之間的排斥作用,因此顆粒可以更好地聚集最終得以沉淀,同時當反離子之間相互吸附時又可以降低膠體之間表面的電荷,直至降為0,甚至可以使離子之間帶相反的電荷,再次增加了粒子之間的排斥作用,因此膠體得以再次穩定;混凝劑之間具有線性結構,具有能和顆粒表面發生化學反應的基團,形成的這些基團能夠把顆粒與混凝劑高效的連接起來,混凝劑與膠體表面的作用主要是因為膠體表面與不帶電的物質之間的范德華力而產生吸附架橋作用;卷掃作用主要是對混凝劑以而言的,這些混凝劑添加到廢水中會發生水解,并生成沉淀,由于沉淀數量和表面積極大,因此之間會有孔網,而部分懸浮物會被吸附到孔網里面而得以去除。目前,廣為應用的混凝劑主要有無機混凝劑、有機混凝劑、微生物以及符合混凝劑。
2.2 沿程SS濃度去除分析
裝置運行穩定后各池子中SS濃度以及各池子中SS的去除率變化曲線見圖2。
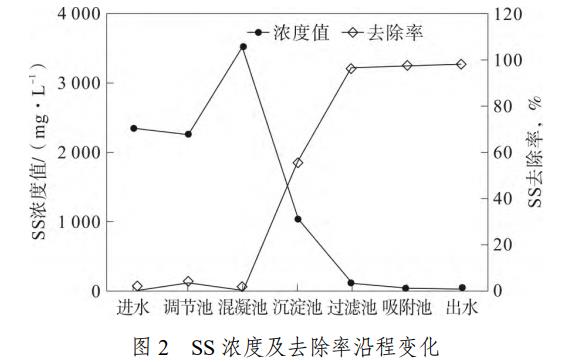
分析可知,進水中SS濃度值為2357.4mg·L-1,調節池中SS濃度值為2263.7mg·L-1、去除率為3.97%;混凝池中SS濃度值為3526.1mg·L-1,遠大于進水中SS濃度;混凝池中SS濃度為3526.1mg·L-1、去除率為55.36%;沉淀池中SS濃度為1052.4mg·L-1、去除率為55.36%;過濾池中SS濃度為125.6mg·L-1、去除率為96.47%;吸附池中SS濃度為41.5mg·L-1、去除率為98.24%;出水中SS濃度為2263.7mg·L-1、去除率為98.41%。因進水水質和水量波動較大,調節池主要是調節水量和水質的,故廢水流經調節池后SS濃度值幾乎沒有變化,只有一些粒徑較大的懸浮物在池內運動過程中通過沉淀得以去除;在混凝池中由于添加了混凝劑和助凝劑,該物質投入水中后本身就會形成沉淀,顆粒物被吸附進入混凝劑形成的沉淀中,由于此時還來不及沉淀,故廢水流經混凝池后SS濃度值升高明顯,遠大于進水中SS濃度值;廢水流經沉淀池后在混凝池中形成的沉淀很快被沉淀下來,故此時SS濃度下降明顯,去除率達到55.3%;一些細小粒徑的SS由于重量不夠在沉淀池無法沉淀,進入過濾池后這些SS被截留下來,故在過濾池中大部分SS被截留下來,SS濃度值又大大下降,從沉淀池至過濾池SS去除率增加了41.11%,吸附池主要是吸附少數過濾池中未過濾完全的極細小顆粒,故SS濃度變化不明顯,從過濾池至吸附池SS去除率僅增加了1.77%。
2.3 Ca(OH)2添加量試驗結果及分析
絮凝的作用主要是使一些膠體粒子或者較小的懸浮物凝聚,且主要是正對不溶于水的物質,由于煤礦廢水中的Ca2+、Mg2+以及SO42-都是水溶性物質,故直接添加混凝劑作用效果不大,故應在混凝劑投入之前先添加適量的熟石灰(Ca(OH)2),Ca(OH)2可以和水中的Mg2+以及SO42-形成CaSO4和Mg(OH)2沉淀,廢水中會產生一定量的CO2,該氣體也可與Ca(OH)2可生成CaCO3沉淀,有了這些沉淀后會使SO42-的絮凝作用大大增強,故為探討Ca(OH)2最適宜的添加量共進行兩組試驗(PAC和PAF試驗),試驗前先調節廢水pH至7左右,保證實驗室氣溫在25℃,每組試驗又分為7小組,每小組用燒杯盛水1L,分別添加濃度為0、0.2、0.4、0.6、0.8、1.0、1.2g·L-1的Ca(OH)2,在7個PAC試驗中各添加30mg·L-1的PAC,7個PAF試驗中各添加30mg的PAF,控制攪拌速度約150r/min,攪拌約2min,開始絮凝時控制攪拌速度為20r/min,控制絮凝時間為10min,隨后靜止20min,取上清液測量水中總硬度以及SO42-含量,各物質含量及試驗現象見表3,不同Ca(OH)2投加量下總硬度以及SO42-去除率曲線如圖3和圖4。
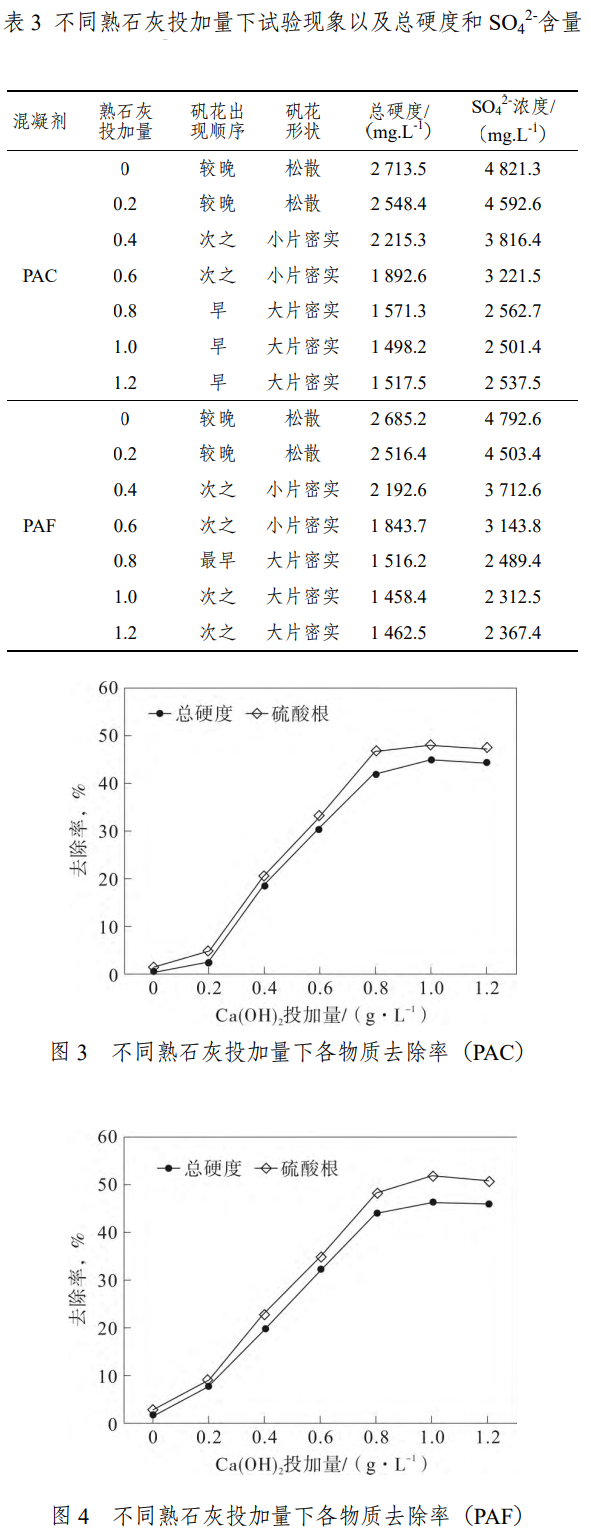
從圖3分析可知:添加PAC混凝劑時,在不添加Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為0.4%,SO42-去除率為1.37%;當添加濃度為0.2g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為6.46%,SO42-去除率為4.66%;當添加濃度為0.4g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為18.69%,SO42-去除率為20.78%;當添加濃度為0.6g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為30.53%,SO42-去除率為33.13%;當添加濃度為0.8g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為42.33%,SO42-去除率為46.8%;當添加濃度為1g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為45.01%,SO42-去除率為48.07%;當添加濃度為1.2g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為44.3%,SO42-去除率為47.33%。
從圖4分析可知:添加PAF混凝劑時,在不添加Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為1.44%,SO42-去除率為0.51%;當添加濃度為0.2g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為7.64%,SO42-去除率為6.52%;當添加濃度為0.4g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為19.52%,SO42-去除率為22.93%;當添加濃度為0.6g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為32.33%,SO42-去除率為34.74%;當添加濃度為0.8g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為44.35%,SO42-去除率為48.32%;當添加濃度為1g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為46.67%,SO42-去除率為52.01%;當添加濃度為1.2g·L-1的Ca(OH)2時,相比進水中濃度,混凝過程總硬度去除率為46.32%,SO42-去除率為50.86%。
圖3和圖4均說明當不添加Ca(OH)2時,總硬度和SO42-幾乎無去除,隨著Ca(OH)2濃度的增加,兩物質的去除率均呈逐漸增大,至Ca(OH)2濃度為1g·L-1時,上升趨勢差不多停止,說明當Ca(OH)2濃度為1g·L-1時為最佳投藥量。
2.4 混凝劑投加量試驗結果與分析
上節中已得出Ca(OH)2最佳投藥量為1g·L-1,故為保證單一變量,控制Ca(OH)2濃度為1g·L-1,改變PAC和PAF的用量,試驗分為兩組,一組添加PAC,另一組添加PAF,每組試驗又分為7小組,每小組用燒杯盛水1L,第一組分別添加濃度為15、20、25、30、35、40、45mg·L-1的PAC,另一組分別添加濃度為15、20、25、30、35、40、45mg·L-1的PAF,控制攪拌速度約150r/min,攪拌約2min,開始絮凝時控制攪拌速度為20r/min,控制絮凝時間為10min,隨后靜止20min,取上清液測量水中總硬度以及SO42-含量,各物質含量及試驗現象見表4,不同Ca(OH)2濃度為1g·L-1時不同PAC和PAF投加量下總硬度以及SO42-去除率曲線如圖4和圖5。
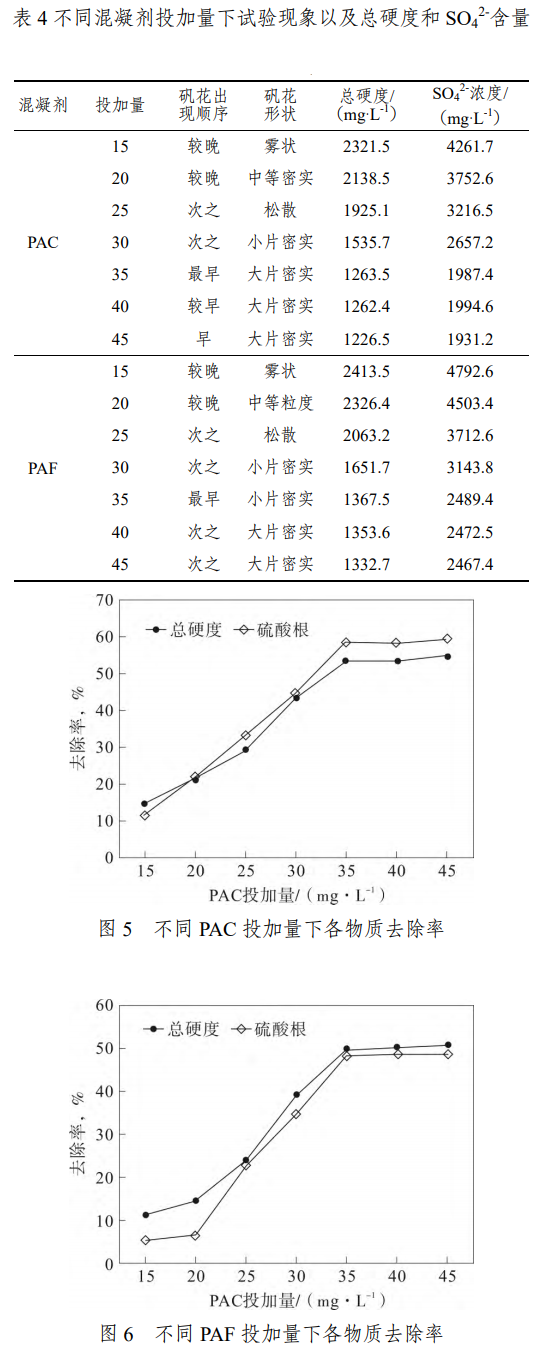
從圖5分析可知:Ca(OH)2濃度為1g·L-1下,當添加PAC為15mg·L-1時,相比進水中濃度,混凝過程總硬度去除率為14.79%,SO42-去除率為11.53%;當添加濃度為20mg·L-1的PAC時,相比進水中濃度,混凝過程總硬度去除率為21.51%,SO42-去除率為22.1%;當添加濃度為25mg·L-1的PAC時,相比進水中濃度,混凝過程總硬度去除率為29.34%,SO42-去除率為33.26%;當添加濃度為30mg·L-1的PAC時,相比進水中濃度,混凝過程總硬度去除率為43.64%,SO42-去除率為44.85%;當添加濃度為35mg·L-1的PAC時,相比進水中濃度,混凝過程總硬度去除率為53.63%,SO42-去除率為58.75%;當添加濃度為40mg·L-1的PAC時,相比進水中濃度,混凝過程總硬度去除率為53.66%,SO42-去除率為58.59%;當添加濃度為45mg·L-1的PAC時,相比進水中濃度,混凝過程總硬度去除率為54.98%,SO42-去除率為59.91%。
從圖6分析可知:Ca(OH)2濃度為1g·L-1下,當添加PAF為15mg·L-1時,相比進水中濃度,混凝過程總硬度去除率為11.43%,SO42-去除率為5.12%;當添加濃度為20mg·L-1的PAF時,相比進水中濃度,混凝過程總硬度去除率為14.61%,SO42-去除率為6.52%;當添加濃度為25mg·L-1的PAF時,相比進水中濃度,混凝過程總硬度去除率為24.28%,SO42-去除率為22.93%;當添加濃度為30mg·L-1的PAF時,相比進水中濃度,混凝過程總硬度去除率為39.36%,SO42-去除率為34.73%;當添加濃度為35mg·L-1的PAF時,相比進水中濃度,混凝過程總硬度去除率為49.81%,SO42-去除率為48.32%;當添加濃度為40mg·L-1的PAF時,相比進水中濃度,混凝過程總硬度去除率為50.32%,SO42-去除率為48.68%;當添加濃度為45mg·L-1的PAF時,相比進水中濃度,混凝過程總硬度去除率為51.08%,SO42-去除率為48.08%。
圖5和圖6均說明隨著投加的PAC或PAF混凝劑濃度的增加,兩物質的去除率均呈逐漸增大,至當PAC和PAF濃度均為35mg·L-1時,上升趨勢差不多停止,說明當混凝劑濃度為35mg·L-1時為最佳投藥量。
3、結語
本文以山西朔州懷仁礦區廢水作為研究對象,采用自行設計的混凝工藝,研究了混凝工藝處理該礦區廢水時需投加的最佳用量,結果表明:
(1)相比進水,SS濃度在調節池變化,經混凝池后SS濃度增大較多,SS的去除主要是在沉淀池和過濾池中,這兩個反應池內SS的去除率分別為55.36和96.47%。
(2)當添加PAC或者PAF為混凝劑時,煤礦廢水總硬度和SO42-的去除率隨投加的Ca(OH)2濃度的增加而增大,當Ca(OH)2濃度為1g·L-1時為最佳投藥量;
(3)隨PAC和PAF濃度的增加,廢水中總硬度和SO42-的去除率逐漸增大,當PAC和PAF投加量均為35mg·L-1時為最佳投藥量。
(來源:中國煤炭地質總局)

禹州華德環保科技有限公司(“雙發壓濾機”)
138 4989 1920
shuangfa2004@163.com
m.bjxlws.com
河南省許昌市禹州市潁川辦產業集聚區東產業園潁川大道南段路東


